Прививка от фентанила: как вакцина может стать первым превентивным оружием против опиоидной эпидемии

В ближайшие месяцы начнутся клинические испытания на людях вакцины, способной блокировать действие фентанила, включая его смертельную передозировку. Это может стать первым в истории превентивным методом лечения расстройства, связанного с употреблением опиоидов.
Первоначальные испытания будут сосредоточены на оценке безопасности вакцины, первоначальная разработка которой велась при финансировании Министерства обороны США. Препарат уже показал многообещающие результаты в испытаниях на крысах. Теперь права на него принадлежат стартапу ARMR Sciences, который начнёт набор пациентов для испытаний I фазы в Нидерландах в 2026 году, ориентировочно в январе или феврале.
«Наша цель как компании — устранить смертельную опасность, исходящую от наркотиков на рынке, — заявил соучредитель и генеральный директор ARMR Колин Гейдж. — Мы хотим достичь этого, воздействуя на коренную причину не только зависимости, но и, очевидно, передозировки».
Как работает вакцина?
Вакцина работает, не допуская проникновения фентанила в мозг, делая его молекулу мишенью для иммунной системы.
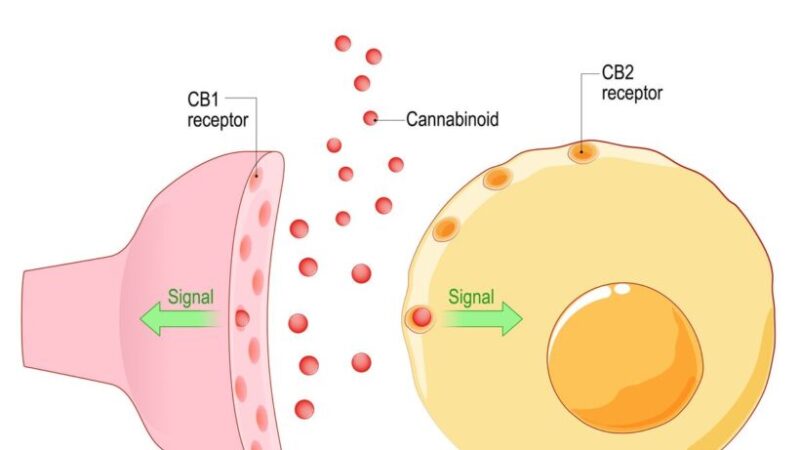
Фентанил — это синтетический опиоид, действие которого в 50 раз сильнее героина. Опиоиды, также называемые наркотическими анальгетиками, в целом работают, связываясь с опиоидными рецепторами в головном и спинном мозге, вызывая изменения в передаче сигналов нервными клетками, которые снимают боль и могут создавать состояние эйфории.
Однако эти же рецепторы находятся в части мозга, контролирующей дыхание, поэтому фентанил при передозировке может угнетать дыхание до смертельного уровня. По данным Управления по борьбе с наркотиками США (DEA), доза всего в 2 миллиграмма фентанила — примерно объём дюжины крупинок соли — может быть смертельной.
Если человек, передозировавший фентанилом, получает налоксон (известный под торговой маркой Narcan) достаточно быстро, эти эффекты можно обратить. Этот антидот также связывается с опиоидными рецепторами, блокируя действие фентанила.
Вакцина ARMR использует другой подход: она действует в кровеносной системе, ещё до того, как наркотик достигнет мозга.
«Это станет первым в истории лечением, которое не воздействует на [опиоидный] рецептор», — пояснил Гейдж.
Из чего состоит вакцина?
Чтобы не допустить фентанил до мозга, иммунная система должна сначала его распознать. Но фентанил — это крошечная молекула, а не патоген вроде вируса, и иммунные клетки естественным образом на него не реагируют.
Чтобы вызвать иммунный ответ на фентанил, команде учёных под руководством Коллина Хейла, соучредителя и научного консультанта ARMR из Университета Хьюстона, пришлось «привязать» опиоид к чему-то другому.
Они выбрали деактивированный токсин дифтерии под названием CRM197 — соединение, уже используемое в некоторых зарегистрированных вакцинах. После деактивации токсин перестаёт быть ядовитым и вместо этого помогает стимулировать иммунный ответ. Чтобы усилить этот ответ ещё больше, они также добавили dmLT — соединение, полученное из токсинов бактерии Escherichia coli. Это модифицированное соединение само по себе не токсично и также тестировалось на людях в рамках испытаний других, ещё не одобренных вакцин.
Эти два компонента присоединены к синтетическому фрагменту молекулы фентанила, который сам по себе не может вызвать ни эйфории, ни обезболивания.
Когда иммунная система сталкивается с этим «коктейлем» из фрагментов фентанила, CRM197 и dmLT, она вырабатывает антитела, реагирующие на настоящий фентанил. Эти антитела связывают опиоид, не позволяя ему пересечь защитную мембрану мозга — гематоэнцефалический барьер — и затем выводят его из организма.
В исследованиях на крысах вакцина блокировала проникновение фентанила в мозг грызунов, а также предотвращала угнетение дыхания и передозировку.
Как тестируют вакцину?
До сих пор исследования вакцины проводились на грызунах, хотя dmLT и CRM197 уже тестировались на людях в той или иной степени и используются в других вакцинах. Протокол для крыс включает начальную дозу вакцины против фентанила с последующими бустерными дозами через три и шесть недель после первой, пояснил Хейл.
«Максимальный срок наблюдения за животными в наших исследованиях составил около шести месяцев, и мы наблюдали полную блокаду эффектов фентанила через полгода после первоначальной вакцинации», — сказал Хейл. Он отметил, что ещё предстоит выяснить, как это переведётся на «человеческие годы», но лабораторные крысы живут в общей сложности пару лет, поэтому исследователи полагают, что вакцина будет действовать на людей долго.
Первые испытания на людях, которые начнутся в начале 2026 года, включат 40 человек и будут сосредоточены на выявлении любых проблем с безопасностью вакцины, таких как нежелательные или опасные побочные эффекты. Исследователи также будут брать у участников образцы крови, чтобы убедиться, что вакцина стимулирует выработку антифентаниловых антител.
Если испытания I фазы будут успешными, следующим шагом станут испытания II фазы для проверки эффективности вакцины — насколько хорошо она блокирует действие фентанила. В этих испытаниях не только будут отслеживать уровень антител с течением времени, но и некоторым участникам под тщательным наблюдением будут вводить безопасные дозы фентанила, используемые для обезболивания при медицинских процедурах. Это позволит проверить, работает ли вакцина в присутствии наркотика.
Есть ли у вакцины потенциальные недостатки?
Фентанил имеет законное медицинское применение в качестве обезболивающего, особенно в экстренных ситуациях. Одна из проблем, связанных с вакциной, заключается в том, что привитые люди могут лишиться этого варианта обезболивания.
Однако, по словам Хейла, антитела, вырабатываемые в результате вакцинации, не связываются с другими опиоидами — такими как морфин, оксикодон или метадон — или с другими вариантами обезболивания. Это означает, что у привитых людей останутся альтернативы, если в будущем им понадобится обезболивание.
Вакцина также не взаимодействует с бупренорфином — препаратом, используемым для лечения опиоидной зависимости путём снижения симптомов отмены и тяги. Хейл сообщил, что его команда в настоящее время тестирует вакцину в комбинации с налтрексоном, неопиоидным препаратом, который также используется для блокировки действия опиоидов при лечении зависимости.
Теоретически возможно принять такое количество фентанила, которое преодолеет запас антифентаниловых антител в организме, отметил Хейл. Однако, учитывая, что вакцина блокирует эйфорический эффект фентанила, он ожидает, что люди, желающие бросить, не будут мотивированы пытаться её «обойти».
«Мы хотим помочь людям, которые хотят бросить, которые не хотят больше употреблять наркотик, — сказал он. — Это даст им шанс осознать, что они не получат кайфа от этого вещества, и в его приёме больше нет смысла».
Кому может быть полезна вакцина против фентанила?
Гейдж предположил, что одним из рынков для вакцины могут стать спасатели и медики, обеспокоенные случайным воздействием фентанила. (Эта обеспокоенность возросла в последние годы на фоне распространения дезинформации о фентаниле).
Для ясности: если фентанил попадёт на кожу при обычном контакте — например, если прикоснуться к объекту, на котором есть следы наркотика, — он не всосётся через кожу. Для значимого всасывания через кожу требуется прямой и длительный контакт с препаратом в течение часов или дней. Тем не менее, если парамедик или полицейский получит препарат на руки, а затем прикоснётся ко рту или глазам, он может почувствовать некоторые анальгезирующие (обезболивающие) эффекты, пояснил Хейл.
Вакцина также может стать «дополнительным инструментом в арсенале» для людей с опиоидной зависимостью, считает Гейдж. Сочетание вакцины с «интенсивной» когнитивно-поведенческой терапией (вид разговорной терапии) и социальной поддержкой может быть «невероятно полезным для людей, которые просто ищут ещё один спасательный круг, чтобы помочь себе выздороветь», — сказал он.
Наконец, вакцина может принести пользу людям, употребляющим менее смертоносные наркотики — такие как кокаин, стимуляторы или обезболивающие, — которые они покупают на чёрном рынке. Всё чаще эти вещества разбавляют фентанилом, а значит, люди могут получить передозировку, даже не подозревая, что принимают опиоид.
«Два моих близких друга детства погибли от передозировки фентанила, — поделился Гейдж. — Ни один из них его не искал».
Согласно предварительным данным, в 2024 году в США от передозировки опиоидами, по оценкам, умерло более 48 000 человек. Возможно, именно из-за таких высоких показателей смертности первые исследования показывают, что люди, имеющие личный опыт опиоидной зависимости, а также широкие слои населения положительно относятся к потенциальной антифентаниловой вакцине. Время покажет, как новая вакцина проявит себя в испытаниях на людях, но если она в конечном итоге будет одобрена, это станет первым в своём роде инструментом в борьбе со смертями от передозировок.
Важное замечание
Разработка такой вакцины поднимает и ряд этических вопросов. Например, как обеспечить справедливый доступ к лечению для наиболее уязвимых слоёв населения? Не станет ли вакцинация формой принуждения для определённых групп (например, для лиц, находящихся в системе уголовного правосудия)? И наконец, может ли создание «иммунитета» к одному опиоиду необоснованно снизить бдительность в отношении общего риска зависимости, подтолкнув к употреблению других веществ? Эти вопросы потребуют тщательного общественного обсуждения по мере продвижения исследований.
Данная статья предназначена исключительно для информационных целей и не является медицинской рекомендацией.